

科普文章
联合用药为既往对PD-1有反应的复发NSCLC患者的治疗提供解决方案
临床研究结果显示(WJOG9616L),对既往PD-1有应答且有足够无PD-1间期的晚期非小细胞肺癌(NSCLC)患者,一旦获得耐药,再次使用纳武利尤单抗(Nivolumab)治疗的疗效相当有限[1]。联合治疗通过多种药物组合协同发挥抗肿瘤作用,为复发/晚期的癌症患者提供更佳治疗手段。利用免疫激动剂与PD-1联合用药治疗既往对PD-1有反应的复发NSCLC患者方案有望惠及更多癌症病人。
研究目的:
在免疫检查点抑制剂(PD-1)治疗有效且有足够长时间PD-1间期的晚期非小细胞肺癌(NSCLC)患者中,探讨再次进行PD-1治疗的疗效。
患者和方法:
该研究前瞻性的纳入了在疾病进展前接受过PD-1治疗,达到完全缓解(CR)、部分缓解(PR)或疾病稳定≥6个月的晚期NSCLC患者(入组前均有≥60天的无PD-1间期)。给予患者纳武利尤单抗(240 mg,Q2W)治疗,直至疾病进展。主要终点为总缓解率(ORR),次要终点包括无进展生存期(PFS)、总生存期和安全性。
研究结果:
2017年10月至2020年2月期间,共入组61例患者,其中59例可进行疗效分析。
既往PD-1治疗中,41例患者达到CR或PR。PD-1治疗的中位时间为8.1个月,中位无PD-1间期为9.2个月。20例患者发生了需要停用PD-1的免疫相关不良事件(irAE)。
纳武利尤单抗再次治疗的ORR为8.5%,中位PFS为2.6个月,其中5例应答者的中位PFS为11.1个月。在多变量分析中,无PD-1间期是PFS的唯一预测因素,而与既往疗效或irAE史无关。常见不良事件包括皮肤疾病(23%)、不适(20%)和低白蛋白血症(15%)。
图1显示了纳武利尤单抗再治疗使肿瘤缩小。5例PR,25例SD,28例进展,1例无法评估。因此,ORR为8.5% (95% CI, 2.8% ~ 18.7%),未达到主要终点。中位PFS为2.6个月(95% CI, 1.6 ~ 2.8个月),12个月PFS率为4.8% (95% CI, 1.0% ~ 13.6%;图2 a)。中位OS为11.0个月(95% CI, 9.0 ~ 14.5个月),12个月OS率为46.4% (95% CI, 32.8% ~ 59.0%)。
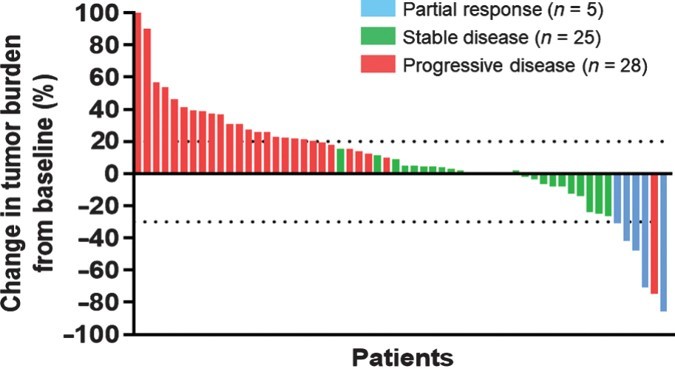
图1.接受纳武利尤单抗再治疗患者的肿瘤负荷瀑布图[1]。
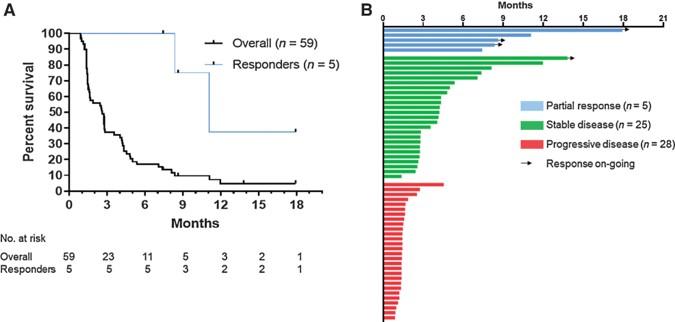
图2.总体患者(黑线,n = 59)和有效患者(蓝线,n = 5)PFS的Kaplan-Meier曲线(A)和Swimmer曲线(B)[1]。
尽管患者数量少,还是有5例PR患者的中位PFS为11.1个月(图2A),并且在分析时大多数患者仍存活(图2B)。如图3所示,无PD-1间期与较长的PFS呈时间依赖性相关。无PD-1时间为2 ~ 6、6 ~ 12、12 ~ 18、18 ~ 24、24 ~ 30个月的中位PFS分别为1.4、1.6、4.3、2.8、8.4个月。
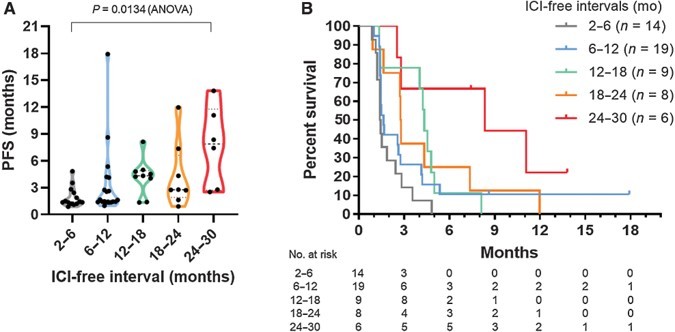
图3. PD-1再治疗时无PD-1间期与PFS的相关性。由于无法收集3例患者既往PD-1的确切完成日期,因此图中总数为56例[1]。
讨论
PD-1单药再治疗的理论依据来源于化疗临床应用的启发,假设化疗敏感的肿瘤细胞最终会通过无药间期复苏,因此即使接受过一线化疗,小细胞肺癌患者的二线治疗仍可考虑化疗。然而,目前尚未研究PD-1再治疗是否可在对既往PD-1有效且在无PD-1间期后的患者中显示疗效。多项研究已经证明了NSCLC患者发生irAEs(免疫检查点药物副作用)后再次接受PD-1治疗的安全性,但其疗效尚未得到充分评估。
一项纳入18例NSCLC患者(包括PD-1有反应者和无反应者)的回顾性病例系列研究表明,再次使用PD-L1抑制剂治疗无效。
与此同时,对III期研究进行的事后分析表明,帕博利珠单抗再次治疗的ORR为15% ~ 33%。需要指出的是,后一份报告中的参与者具有高度选择性,因为他们只有在完成2年的帕博利珠单抗治疗后才允许再次接受帕博利珠单抗治疗。患者人群的这种异质性导致很难确切阐明最终结果。
关键纳入标准主要符合PD-1获得性耐药的定义:70%的患者在之前的PD-1治疗中达到CR/PR,中位无PD-1间期为9.2个月。试验结果提示,即使之前的PD-1显示出一段时间的应答,PD-1再次治疗并不是有效的治疗方法。亚组分析显示,具有非鳞状细胞癌、PD-1治疗时间长、无PD-1间期长、有irAE病史的患者PFS更长,多变量分析发现:在以上这些因素中,较长的无PD-1间期是PFS改善的唯一预测因素。随着无PD-1间期的延长,PFS显著延长(图3)。提示我们,足够的无PD-1间期可能为PD-1再治疗获得疗效提供线索,但最佳持续时间仍未知。此外,即使无PD-1间期为24 ~ 30个月的患者有8.4个月的中位PFS,也不能否认其肿瘤只是缓慢进展的可能性。
总之,即使在最初对既往PD-1有应答且有足够无PD-1间期的患者中,一旦获得耐药,再次使用纳武利尤单抗治疗的疗效非常有限。只有一小部分患者达到持久缓解,因此开发新的联合治疗方案是必要的。
礼进生物,一家全球领先致力于开发和商业化first-in-class 和 best-in-class的肿瘤生物药物的创新型生物技术公司,正在计划开展一项开放标签多中心随机的临床II期试验,评估LVGN7409 联合BMS纳武利尤单抗注射液或多西他赛对晚期/转移性非小细胞肺癌(NSCLC)的疗效和安全性。通过联合用药的方式,协同发挥免疫激活和肿瘤抑制杀伤作用,以期惠及更多复发/难治性癌症患者。
LVGN7409是一种重组单克隆抗体,可选择性地在肿瘤微环境中高效激活CD40,CD40是肿瘤坏死因子(Tumor Necrosis Factor, TNF)受体家族的成员之一,又称TNFRSF5。CD40的激活将促进肿瘤抗原呈递,逆转肿瘤微环境对免疫的抑制,恢复免疫系统的抑瘤功能。
纳武利尤单抗是一种针对程序性死亡 1(PD-1)受体的人源化单克隆抗体,阻断其与PD-L1和PD-L2的相互作用,释放被PD-1通路抑制的包括抗肿瘤功能在内的免疫反应。
多西他赛是一种用于治疗多种癌症的抗微管蛋白化疗药物,适应症包括非小细胞肺癌、乳腺癌、头颈癌、胃癌和前列腺癌。
“礼进生物相信,直接激活CD40和解除PD-1抑制的联合治疗极有可能提升肿瘤免疫治疗效果,即LVGN7409和免疫检查点抑制剂的联合使用,预计在耐药和复发患者中显示出优异的协同作用,进一步验证我们临床前研究成果” 礼进生物首席医学官詹宗晃博士强调。“我们也相信,LVGN7409可能在与多西他赛等有免疫调节功能的化疗药物的联合方案中发挥作用。通过这项II期研究,我们希望证明CD40的激活可以逆转导致耐药的免疫抑制肿瘤微环境,通过与现有标准治疗联合用药的方式提高疗效。难治性非小细胞肺癌有很大的临床未满足需求,我们希望给予这类患者提供更有效的治疗方案。”詹博士补充道。
本文仅作信息分享,不代表礼进生物公司立场和观点,也不作治疗方案推荐和介绍。如有需求,请咨询和联系正规医疗机构。
参考文献
1. Akamatsu, H., et al., Nivolumab Retreatment in Non–Small Cell Lung Cancer Patients Who Responded to Prior Immune Checkpoint Inhibitors and Had PD-1-Free Intervals (WJOG9616L). Clinical Cancer Research, 2022. 28(15): p. 3207-3213.
2. lyvgen news release: https://www.lyvgen.cn/bms-lyvgen
礼进生物(Lyvgen Biopharma)的网站(中文)
礼进生物创建于2016年,以其全球创新的肿瘤免疫激动性抗体管线为核心,凭借其世界级的研发团队,最前沿的药物研发项目,以及开放式创新的策略, 有望引领国内新药研发行业走向全球。
https://user-assets.sxlcdn.com/images/676507/FiTA8WK-FQRyXrQDyd-HDkY3tpfI.png?imageMogr2/strip/auto-orient/thumbnail/1200x630>/format/png




 沪公网安备 31011502015333号
沪公网安备 31011502015333号